Des protéines flexibles pour assembler les virus : du désordre à la symétrie.
Des chercheurs et chercheuses ont expliqué le mécanisme grâce auquel des protéines identiques parviennent à s’organiser et former les capsides parfaitement symétriques de la plupart des virus.
Références :
Siyu Li et al., From disorder to icosahedral symmetry: How conformation-switching subunits enable RNA virus assembly. Sci. Adv. 11, ealy7241 (2025).
DOI : 10.1126/sciadv.ady7241
Archive ouverte HAL
Les virus à ARN simple brin (ssARN) représentent la famille de virus la plus grande et la plus diversifiée que l’on connaisse, touchant les humains, les animaux et les plantes. Leur formation repose sur un phénomène fascinant : des centaines de protéines identiques s’auto-assemblent spontanément pour former la coque protectrice du virus, appelée capside, adoptant souvent une symétrie icosaédrique d’une précision remarquable. Pourtant, malgré des décennies de recherche, les mécanismes physiques et moléculaires qui gouvernent cet auto-assemblage demeuraient mal compris.
Ces recherches ont été menées dans les laboratoires CNRS suivants :
Laboratoire de physique des solides (LPS, CNRS / Université Paris-Saclay)
Pour élucider ce processus, des chercheurs et chercheuses d’une collaboration franco-américaine impliquant le LPS ont développé un modèle de dynamique moléculaire novateur, combinant des éléments essentiels de la physique et de la biologie, à savoir la diffusion des protéines, la flexibilité du génome viral, et un mécanisme de commutation conformationnelle imitant l’allostérie, cette capacité qu’ont certaines protéines à changer de forme en se liant au site d’une molécule effectrice (qui peut appartenir à la même protéine). Dans ce modèle, chaque sous-unité protéique est capable de changer de forme lorsqu’elle interagit avec une autre, activant des propriétés élastiques qui facilitent la construction d’une coque régulière. Ce comportement flexible – absent des modèles rigides précédents – permet, pour la première fois, de reproduire numériquement la formation spontanée de capsides icosaédriques complètes correspondant aux structures « T=3 » et « T=4 » les plus répandues dans la nature.
Les simulations montrent que l’assemblage ne suit pas un chemin unique mais se produit via plusieurs voies qui débutent en parallèle : des fragments de coque apparaissent simultanément en plusieurs points du génome, puis fusionnent et se réorganisent jusqu’à atteindre une structure parfaitement symétrique. Cette dynamique de « du désordre à la symétrie » révèle le rôle clé de la flexibilité protéique pour franchir les barrières énergétiques qui séparent les états instables des architectures virales ordonnées. Ces résultats ont été validés expérimentalement grâce à des mesures de diffusion des rayons X aux petits angles (SAXS) et de cryo-microscopie électronique (cryo-TEM) sur le virus végétal CCMV (Cowpea Chlorotic Mottle Virus). Les chercheurs ont montré que la structure secondaire de l’ARN influence fortement la réussite de l’assemblage : les ARN plus ramifiés, donc plus compacts, favorisent la formation de coques complètes, tandis que les ARN plus linéaires mènent à des structures incomplètes ou irrégulières.
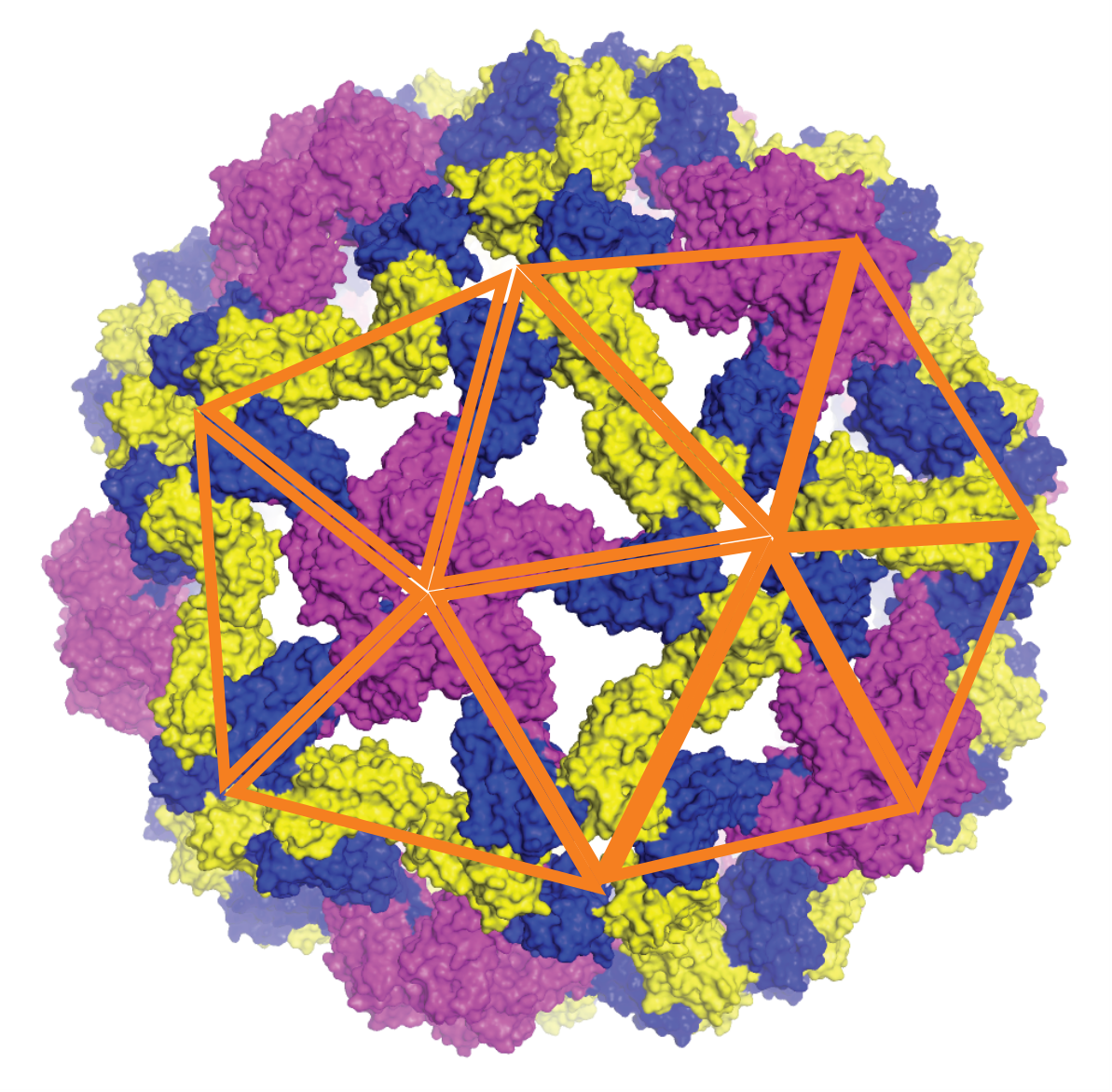
En démontrant que la symétrie virale émerge de principes physiques universels — un équilibre subtil entre propriétés élastiques, forces électrostatiques et architecture du génome —, ce travail fait faire un progrès substantiel dans la compréhension des mécanismes fondamentaux de la virologie. Cette approche fournit un cadre explicatif général pour rendre compte de la formation et la stabilité des capsides, et ouvre ainsi de nouvelles perspectives pour la conception de nano-capsides artificielles destinées à l’encapsulation de molécules thérapeutiques ou à la conception d’agents antiviraux ciblant les étapes précoces de l’assemblage viral. Ces résultats sont publiés dans la revue Science Advances.
Les résultats scientifiques de CNRS Physique
Communiquer sur son résultat scientifique à CNRS Physique
Vous travaillez dans une unité rattachée à CNRS Physique ? Vous pouvez nous proposer vos résultats marquants pour communication. Retrouvez toutes les informations dans la fiche communiquer à CNRS Physique !